药妆史+法规大全
我们之前在多篇文章中提及过“药妆”这个概念,也报道过多个药妆品牌的故事。
在消费升级的当下,我们看到的趋势是:
1、日化线化妆品纷纷开始向有一定功效的药妆产品转型升级。
2、药妆与美业皮肤类服务面对的市场需求高度重合。线下美业机构向来追求为顾客提供更明显的美容效果、更高的服务价值,也已经设定专业药妆作为服务的一部分。
但当我们谈论“药妆”时,我们是否清楚自己到底是在谈论什么?“药妆”到底是像过去一阵风似的一个营销概念,还是一个真正有潜力的美业产品门类?
如果简单把这个问题抛给皮肤科医生或者化妆品销售人员,他们也未必能给出一个清晰的答案,不如随着《美业观察》一起通过这篇文章看透药妆的过去、现在和未来。
文 /《美业观察》 徐佳 发自深圳
药妆是怎么来的?
▷ 我们讲过“皮肤教皇”——奠定了当代皮肤医学多项基础理论的Albert Kligman博士的生平故事,“药妆”能在今天广泛存在于医学界和消费者的心智中,和他有莫大关系。(详情点击《祛痘?抗皱?研究药妆史,当然要从这位“皮肤科教皇”开始……》)

▷ 其实早在1946年就有人首先使用“功效化妆品”的说法,但这个概念清晰地被医学界和化妆品行业广泛接受,一般认为是源于1984年Kligman博士在美国化妆品化学家协会会议上提出了“药妆(cosmeceuticals)”这个词。
▷ 他在发言中用“药妆”来描述唇膏和眼影等化妆品,与抗生素和皮质固醇等药品之间的一类产品。他认为这类产品同时具有化妆品特性(改善容貌)和药品特性(影响皮肤结构和功能)。与普通化妆品/护肤品不一样的是,药妆能够帮助医生,解决患者轻微的皮肤问题。
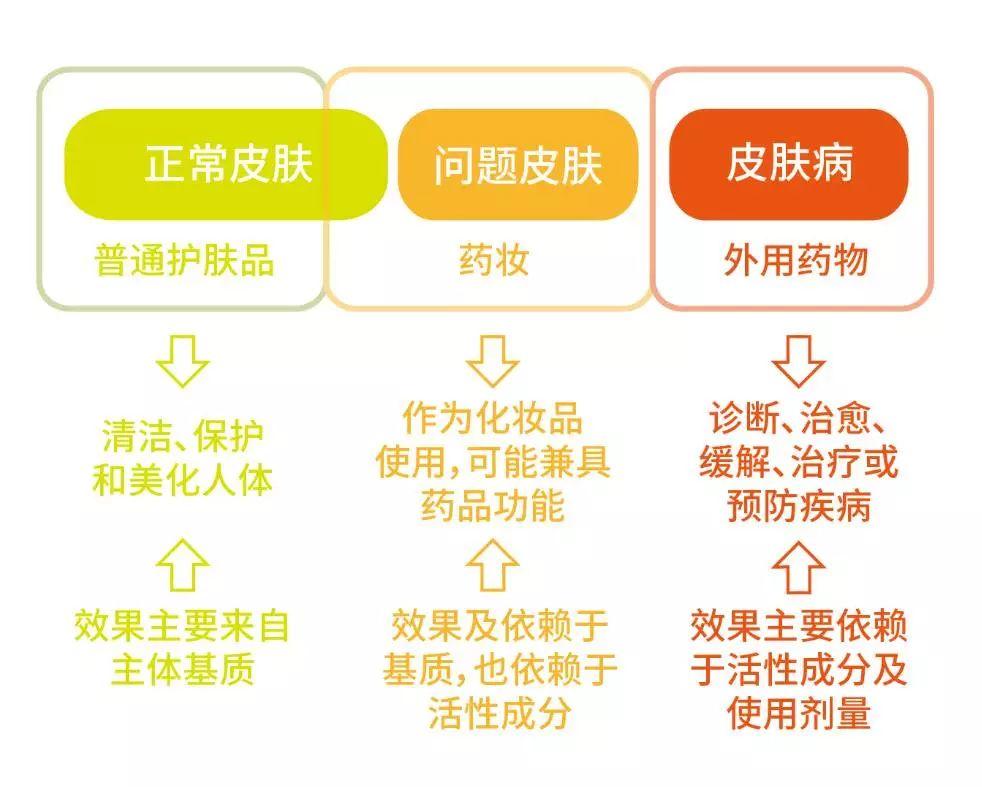
▷ “药妆品的英文单词(Cosmeceutial) 是由化妆品(Cosmetics) 和药品(Pharmaceutials)两者组成的,意思是指具有药物性质的化妆品。药妆品的属性是化妆品,而不是药品,主要用途是美容护肤和促进皮肤健康,解决轻微肌肤问题。”——中国CFDA官网科普文章
世界上第一个药妆是怎么来的?
▷ 第一个被医学界广泛认可的现代药妆是维A酸类药妆。Albert Kligman博士本人发明了皮肤科革命性的处方药:全反式维A酸(Tretinoin)乳膏,商品名Retin-A。
▷ 这种外用处方药物在皮肤科医生手里非常强力,不单能够治疗痤疮,后续还被发现有助于改善皮肤老化、减少皱纹,恢复皮肤的鲜嫩亮泽。
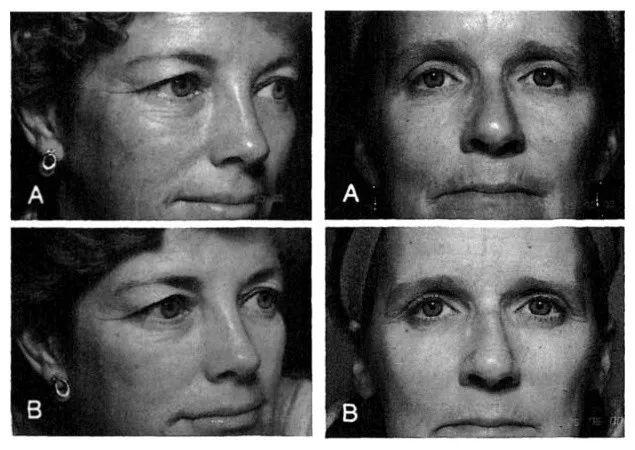
A:治疗前;B:0.05%全反式维A酸乳膏治疗24周后
▷ 通过细胞、动物和多中心随机双盲的临床试验证实,维A酸乳膏能够加速角质层细胞代谢,对抗紫外线引起的皮肤光老化(photoaging)、皱纹等问题时的生物学机制清晰,治疗效果得到了医学界充分认可,在很长一段时间内是FDA批准唯一能够用来使皮肤“年轻化”的药物。但坚持使用这种药膏的女性始终只是广大适用人群中的极少数。
▷ 这是为什么呢?首先因为维A酸类药物治疗痤疮或皮肤衰老不像糖皮质激素,涂上就见效;长期的治疗效果有时需要6个月左右才能充分展现出来。
▷ 而且这个药物对皮肤的刺激性非常强,在治疗前两周左右不少人皮肤涂抹后会产生脱皮、红肿、疼痛甚至出水泡等副作用;如果希望患者坚持使用,必须要皮肤科医生的不断监督和鼓励。
▷ 另外一个因素就是维A酸乳膏没有彩妆即刻美颜的效果,乳膏配方为药物制剂的配方思路,使用体感、气味远远不如普通护肤品中的润肤霜或晚霜,很多女性哪怕知道每天使用带来的益处也难以坚持。
▷ 当时很多皮肤科医生给患者的建议是,把维A酸乳膏混入日常使用的面霜里,在手上抹匀,然后再涂抹到脸上。这样做的好处是药物在脸上的浓度下降,皮肤刺激、红肿脱皮的现象也会减少,而且在发挥药用功效的同时皮肤得到面霜的充分滋润和保湿。于是很快会有人提出这个问题:为什么不生产一种已经含有维A酸的面霜呢?
▷ 由于维A酸是法定的处方药物成分,化妆品行业很快转换思路,把具有类似维A酸功效,但更加温和的、也无需医生处方的维A醇(视黄醇)、维A醛和维A酯类活性物质添加到了化妆品中——这就是第一代“药妆”的诞生。

几款以维A醇(视黄醇)为特色的药妆
▷ 这些来自维生素A酸大家族的成分,同样具有加快皮肤细胞代谢、改善皮肤老化和减少皱纹的效果,但要效果和刺激性要比维A酸温和得多。研究表明,浓度为0.5%的维A醇效果大概等于0.025%的维A酸,也就是说维A醇的效果只相当于维A酸的20分之1。因而,把维A醇加入到面霜等产品使用时,极少带来皮肤刺激或者干燥脱皮等问题。
▷ 这种温和的维A醇或酯类润肤霜如果坚持使用6-18个月,也能够带来类似维A酸乳膏的抗皮肤衰老效果,因而在医生推荐、企业广告的作用下风靡欧美化妆品市场,引领了的第一波抗衰老护肤品浪潮,并且至今是抗衰老药妆的主力成分。
▷ 同样的例子也发生在80年代果酸产品上。传统的化学剥脱嫩肤治疗,需要使用高浓度的果酸或水杨酸等药物。以果酸来说,浓度20%-70%的果酸化学剥脱,要在皮肤科诊所或医院由专业的皮肤科医生进行治疗。
▷ 浓度低于或等于10%的果酸,可以直接加入面霜、洁面等类型的化妆品,日常使用也有一定预防毛孔堵塞、调节皮肤角质代谢、预防痤疮等效果。一个崭新的果酸药妆市场就此打开。

美国某款以10%甘醇酸为活性成分的润肤霜
▷ 总而言之,消费者希望从“药妆”获得的是化妆品的即刻护肤效果,同时也期待它带来类似或接近皮肤科药物/治疗的深度护肤效果。
“医学护肤品”—皮肤科医生眼中的药妆
▷ 大多数皮肤科医生乐见药妆的发展。他们认为这种有功效性的护肤品或化妆品,有助于帮助他们治疗过的患者加速皮肤康复或保持皮肤健康,预防一些治疗后的并发症,比如激光等治疗后,加速皮肤修复或防止额外紫外线损伤。
▷他们把这类产品称之为“功效性护肤品(functional cosmetics)”或“活性护肤品(active cosmetics)”。中国的医生一般将这一类护肤品称为“临床护肤品”或“医学护肤品”。
▷ 有些医生积极地与强生、联合利华等医药或化妆品企业共同投入药妆开发,有的皮肤科医生会自己在诊所调配少量医学护肤品,甚至创立自己的药妆品牌。之前我们报道过的Proactiv和Rodan+Fields就是美国两位皮肤科医生,在业余时间改良了痤疮用药的剂型、气味、质地,提升使用体感后,推向市场打造的药妆品牌。(详情点击《药妆史|电视购物、直销、网宣…只争“下半生”的医生闺蜜创业直登福布斯》)

到底是药还是妆?各国法律如何定义“药妆”
▷ 然而,药妆发展过程中还是遇到了很多实际的问题。西方主要市场和中国大陆的法律对药妆这一类同时具有药物特性和化妆品特性的产品要么完全没有定义,对“药妆”不予承认,要么虽然有所定义,但外延和内涵不统一。我们首先来看看“药妆”概念的发源地美国:
美国
▷ 美国联邦政府对化妆品和药物的管理的主要部门为美国食品药品管理局(FDA)。其授权主要来自1938年通过的《联邦食品、药品和化妆品法》(The Federal Food, Drug & Cosmetic Act )。
▷ 但对于药物和化妆品的区别,该法案给出了明确界限,主要区别来自于预期用途,该法案称“用于诊断、治愈、缓解、治疗或预防疾病的物品”以及“用于影响人或动物的身体结构或任何功能的物品(食品除外)”([FD&C Act, sec. 201(g)(1)])。
▷ “产品可以是药品、化妆品或两者兼而有之”(“A product can be a drug, a cosmetic, or a combination of both)”,如果两者都是,则按药物进行更高要求的监管。同时FDA明确认为“cosmeceuticals”(药妆)这一术语在美国法律下不存在。
▷ 而怎样来确定一个产品的预期用途呢?FDA同时举例说明: “预期用途是治疗或防止疾病或以其他方式影响人体的结构或功能的宣传语都将产品定位为药品。”:
▷ 例如,洗发水因为其预期用途是清洗头发,所以是化妆品。去屑产品因为其预期的用途是治疗头皮屑,所以是药品。去屑洗发水因为其预期用途是清洗头发+治疗头皮屑,所以既是化妆品也是药品,按上述规定要被FDA作为药物监管。
▷ “某些夸张的宣传语可能导致产品被视为药品,即使产品是被当作化妆品出售的。”例如,某些宣传语宣称, 产品能减少脂肪、治疗静脉曲张、增加或减少皮肤中黑色素(色素沉着) 的产生、使细胞再生、使秀发恢复生长等。在宣传中出现这些预期效果描述的产品,不管自己声称是化妆品还是保健品,最后都可能被FDA认定为是药品。
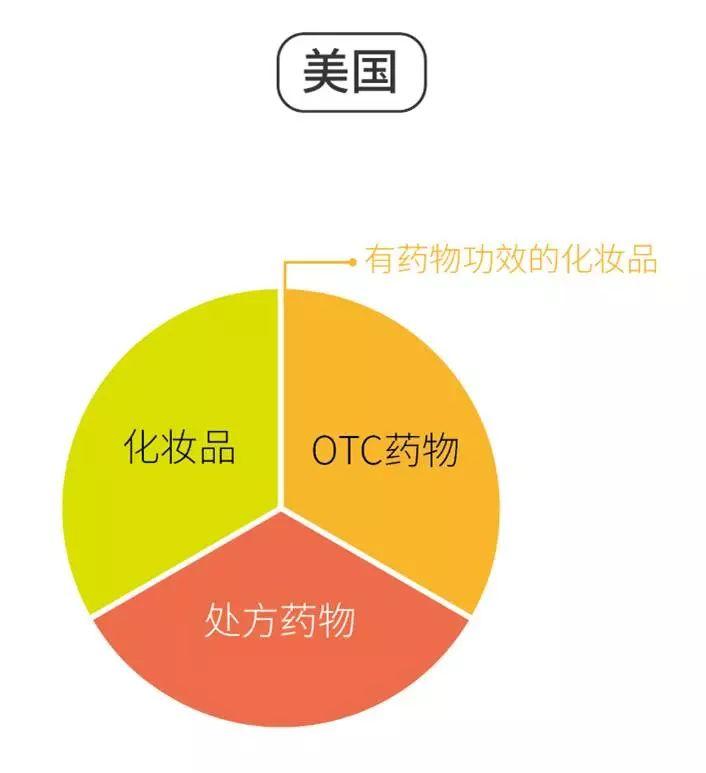
▷ 统计下来,被FDA以OTC药物标准监管的功效性化妆品类别有:
防止粉刺制品;抗细菌制品;抗真菌制品;止汗制品;收敛制品;去头屑制品;除臭制品(外用);防治疱疹和冻疮制品;促进头发生长制品;防止脱发制品;缓解银屑病制品;缓解脂溢性皮炎制品;皮肤漂白制品;皮肤防护制品;
▷ 基本上涵盖了传统意义上的“药妆”范畴,同时也意味着这些产品:按照《联邦食品、药品和化妆品法》,药品在上市前必须获得FDA通过新药上市申请(New Drug Application)程序给予的批准,或符合适用于非处方药审查机构确定的特定药品 “单行规定(monograph)”。
▷ 许多被认为是OTC药品的药妆或含有活性成分的化妆品,如果被认定为是“一般而言安全和有效(Generally Recognized as Safe and Effective, GRSE)、并标注了所有活性成分”则可以按单行规定流程,无需FDA上市前审批就可以销售。
▷ 例如,宝洁公司在美国市场销售的某款带补水+防晒护肤品,看起来像是一款很普通的护肤品:

▷ 实际上在美国的法律地位是OTC药物,只不过是无需通过上市前审批的“单行规定”类别。
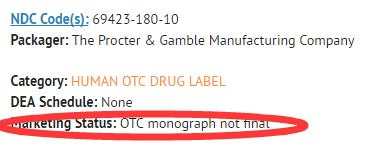
▷ 生产监管:OTC药物生产需按照GMP标准,高于普通化妆品。
▷ 营销宣传规范:化妆品不得使用带有治疗预期的宣传语,宣传的治疗功效需要提交临床试验资料。
欧盟
▷ 欧盟对化妆品进行监管的法律主要为1976年颁布的化妆品指令76/768/EEC。2009年该法律更新为《欧盟化妆品法规EC 1223/2009)》。与美国类似,欧盟法律认为如果一个产品同时具有药品和化妆品的功能,该产品应按照药品进行管理。
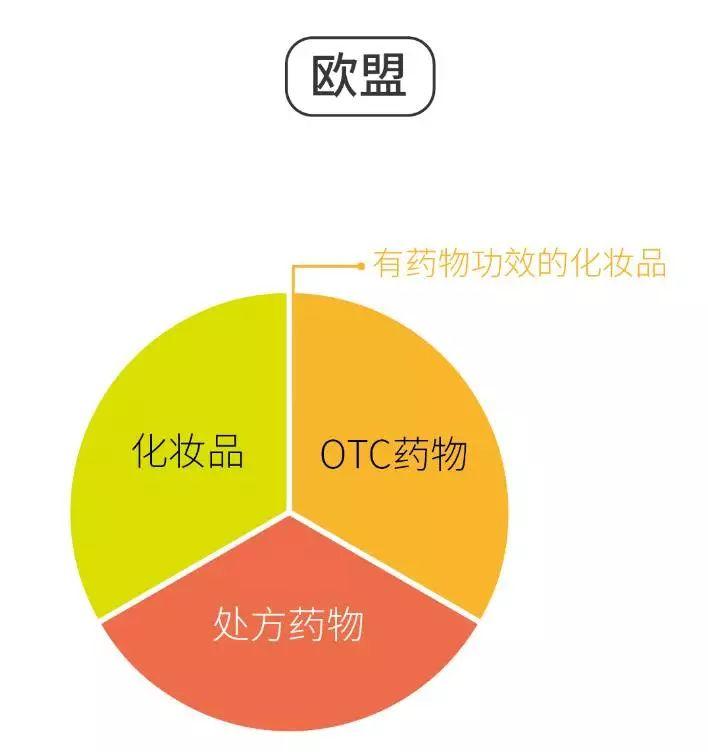
▷ 但与美国不同的是,欧盟对化妆品法律的修订更加及时,也更加具有开放性。截至2016年,EC 1223/2009,修订多达17次。新法规涉及纳米材料、动物实验、原料管理等方面的条款,与产业技术更新联系得更加紧密。
▷ 欧盟各国有相应的执法机构来管理化妆品和药物。以化妆品和药妆大国法国为例,监管药妆市场的部门为法国药品及健康产品卫生安全局(ANSM)。该机构负责:药品行业机构成立前审查,发放市场准入许可,产品上市后跟踪监管,原材料、临床试验和产品质量安全性的把控,广告宣传监管等。
日本
▷ 日本对药物、医药部外品进行监管的主要法律依据是《药事法》,监管主体单位是日本厚生劳动省。
▷ 日本的药品分类非常详细,除了处方药“第1类医药品”之外,还将非处方药分为了“第2类医药品”和“第3类医药品”。
▷ 而且,日本是发达国家中对唯一一个用法律定义了“准药/半药(quasi drug)”概念的国家,单独设立了普通产品和药品之间的“医药品外部”,从而在这一基础上给予了“药妆”法定地位。
▷ 《药事法》将“医药品外部”定义为药物以外有特定使用目的、对人体作用温和、不是器具或器械的产品。在管理上属于药品,然后在销售时不如药品那样严格,任何人都可以购买。
▷ 在医药品外部中有一类是“劳动厚生大臣指定的产品”,可以理解为厚生省特别确认的产品,里面就明确包括“含药化妆品(Medical Cosmetics)”。
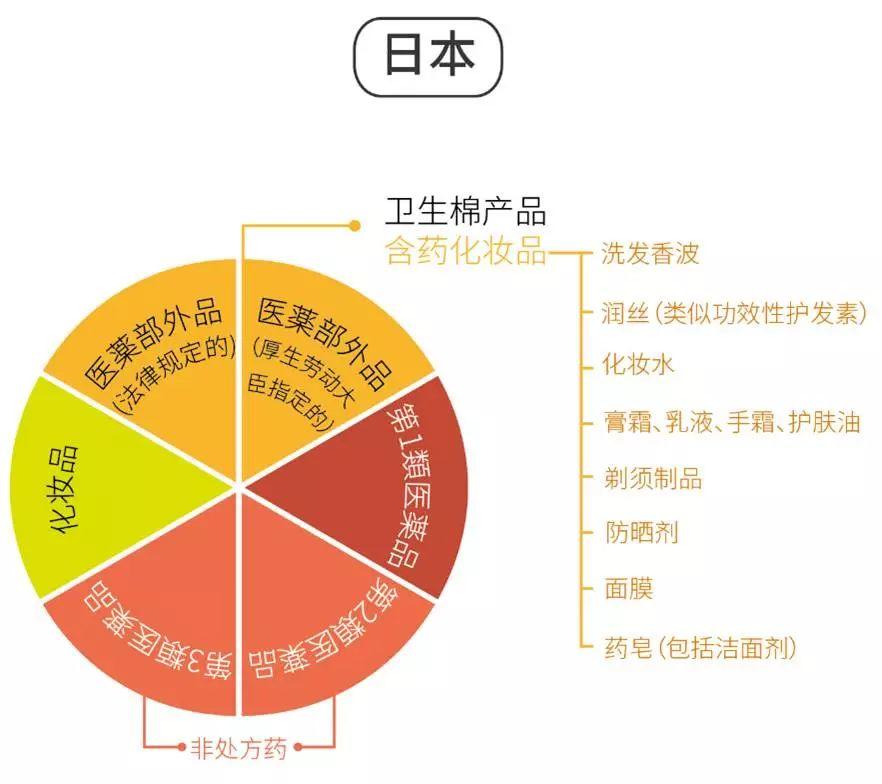
▷ “含药化妆品”作为医药品外部的一种,受到的监管和上市条件与医药品外部一致:
▷ 上市前监管:上市或进口前需申报审批,由厚生劳动省颁发许可。
▷ 生产:GMP标准,高于普通化妆品
▷ 成分:对人体作用温和,以政府审批为准。
中国
▷ 中华人民共和国国家标准—《化妆品卫生标准》于1987年10月1日开始实施。这是我国第一部化妆品卫生质量标准,后来经过二次修订,成为《化妆品卫生规范》。
▷ 我国规范管理化妆品的主要法规是卫生部1989年颁布的卫生部第3号令《化妆品卫生监督条例》,以及1991年颁布实施的《化妆品卫生监督条例实施细则》。后根据我国化妆品行业发展,逐步建立起了一系列化妆品标准、规范和管理及实施条例。其他与化妆品行业直接相关的法规总结如下:

▷ 我国对化妆品的主要管理部门有:
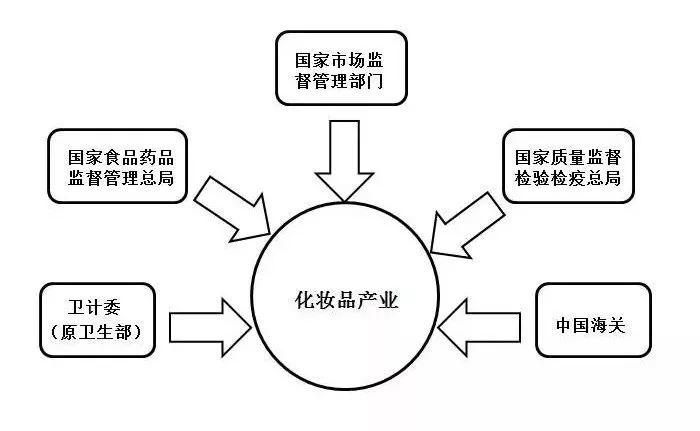
▷ 我国对有治疗功效的化妆品做了独特的区分,《化妆品卫生监督条例》定义了具有育发、染发、烫发、脱毛、美乳、健美、除臭、祛斑、防晒9类功效的化妆品为特殊用途化妆品。
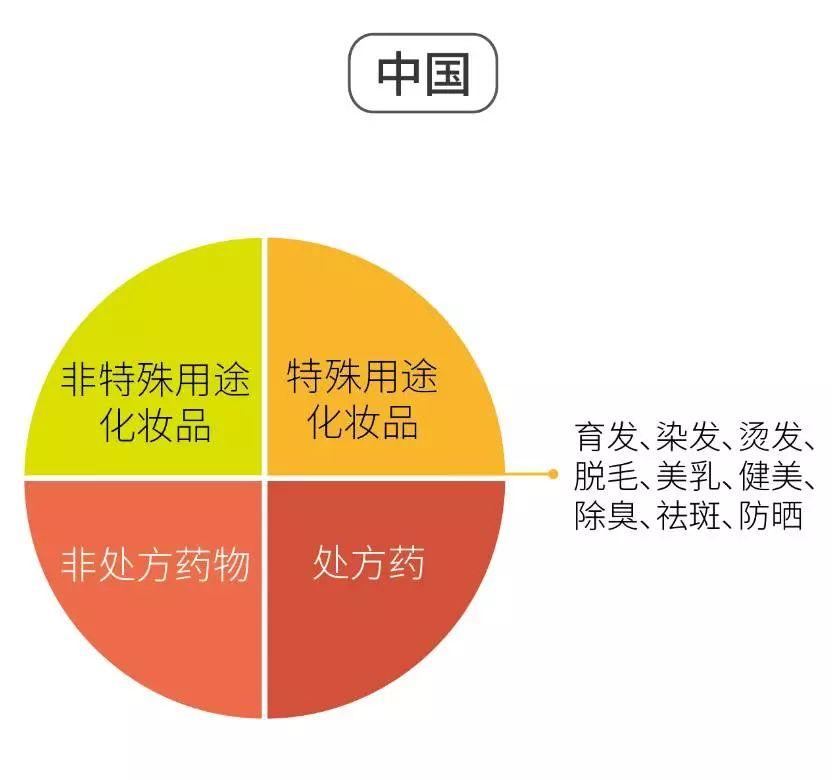
▷ 上市前监管:特殊用途化妆品和非特殊用途化妆品上市前都要通过审批,获得颁发许可证方可生产。
▷ 生产:与普通化妆品一样,无需GMP标准。
▷ 成分:必须来自CFDA定期公布的《化妆品原料名称目录》。
▷ 宣传:国家食药监总局发布的《关于印发化妆品命名规定和命名指南的通知》详细规定了宣称禁用词语和可宣称用词,对几个比较突出的问题做了如下规定:
1)不得使用“医生”等相关词语进行化妆品命名;
2)不得使用“全效”、“高效”、“速效”、“全面”、“极致”、“第一”等绝对化的词语;
3)不得使用“抗菌”、“除菌”等明示或暗示医疗作用和效果的词语;
4)不得使用“药妆”、“医学护肤品”等标识和宣传。
▷ 由此可见,和欧美发达国家一样,“药妆”这个市场概念在我们国家法律体系下并不存在。对具有类似药物功效的化妆品我们用了“特殊用途化妆品”进行特别的管理和规范,国产产品获得“特”字号,进口产品获得“特进”字号许可证方可进行生产和销售。对比美国的单行规范非处方药(OTC monograph)和日本的“医药品外部-含药化妆品”,我国的“特”字号化妆品范围相对较窄,对照消费市场意义上的“药妆”概念差距也更大。
中国的药妆产业未来会如何发展?
▷ 这是不是就意味着,政府监管部门就完全忽视了非法律层面的“药妆”概念呢?CFDA官网于2017年10月发布的一篇文章《什么是药妆品?》对药妆给出了更加清晰的定义:
“药妆品”…“是指具有药物性质的化妆品,药妆品的属性是化妆品,而不是药品,主要用途是美容护肤和促进皮肤健康,解决轻微肌肤问题。”
▷ “药妆品作为一类功能型化妆品,与普通化妆品不同的是,以医学理论为指导(包括西医理论和中医理论),配方设计依据医学思想,针对皮肤问题和皮肤健康需求设计,具有修复皮肤屏障、抗衰、美白、降低刺激源等作用,配方尽量精简,不含有或少含有色素、香精、防腐剂、表面活性剂等,并且具有活性成分含量较高、针对性强、功效显著的特点。”
▷ 可以看出,CFDA这一文章对药妆概念的外延和内涵都做出了更加清晰的界定,从一定层面上也说明了监管部门对当前市场实际情况的认知和未来监管的大体思路。
你手中的药妆其实是什么?
▷ 按照食药监总局官网文章所述:“药妆品的特点有:(1)具有药物活性,可在正常或近似正常的肌肤上使用;(2)产品有改善轻微的皮肤异常的效果,如针对红血丝的药妆品;(3)由于产品针对的是轻度皮肤异常,因此风险性应该极低。”
▷ 这或许会更接近消费者心中的“药妆”。但这一概念在不同国家的法律体系下并没有统一的规范,甚至在医学界和化妆品行业也没有标准。
▷ 以市场的眼光来看,消费者为了改善皮肤状况,在国内或境外购买的一瓶“药妆”,很有可能是除了处方药以外的任何一种类别的产品:(1)普通化妆品;(2)我们国家属于特殊用途的化妆品;(3)美国或欧洲属于OTC药物;(4)从皮肤科诊所或医院购买,属于医院制剂的范畴。
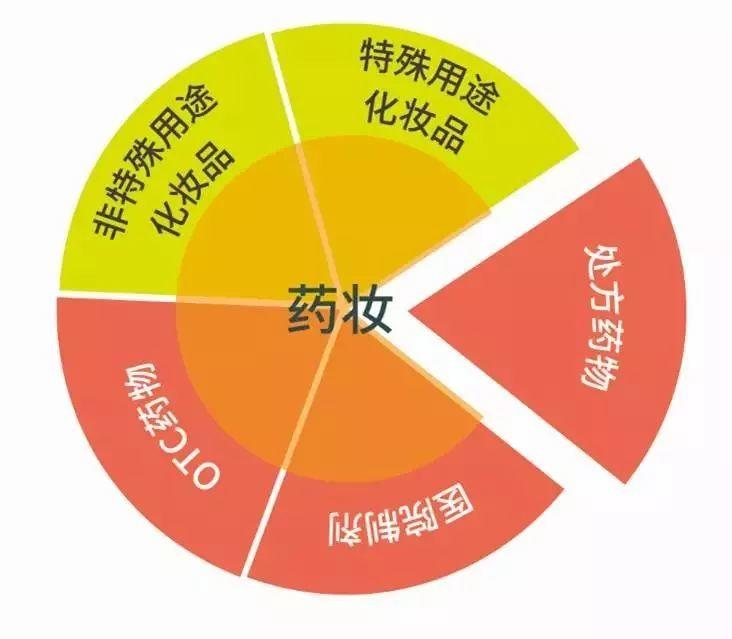
▷ “药妆”从诞生之初,就是皮肤科医生认同,消费者需求明确的特殊品类产品。有皮肤科专家指出“从产品本质来看,药妆品是化妆品产品属性的延伸,它代表了化妆品行业的发展趋势和进步。化妆品的法规管理全球一体化是大势所趋。”
▷ 药妆部门占整个化妆品市场的份额在不断扩大,欧美及新兴市场的药妆细分市场发展速度往往高于整个化妆品行业发展速度。但因为法律定义的含混不清、化妆品界和医学界以及监管部门之间的各种博弈,给药妆的发展带来了一定阻碍。
药妆未来在日本以外的世界主流市场,能不能摆脱身份不清不明的尴尬地位?从药妆过去30多年的的发展中,我们能看到它未来有怎样的发展趋势?2017年中国和世界药妆行业,出现了哪些重大的并购、合资等行业时间?请留意美观君对药妆市场的后续报道。
参考文献:
[1] 裘炳毅,高志红,《现代化妆品科学与技术》,中国轻工业出版社,ISBN:9787518404711
[2] 李利,《美容化妆品学》,人民卫生出版社,第二版
[3] Kligman AM, Grove GL, Hirose R, Leyden JJ, Topical tretinoin for photoaged skin, Journal of the American Academy of Dermatology (1986), Volume 15 Number 4, Part 2, 837
[4] Olsen EA et al., Tretinoin emollient photodamaged skin cream: A new therapy for photodamaged skin. Journal of the American Academy of Dermatology(1992), 26:215-24
[5] Draelos ZD, Cosmeceuticals: undefined, unclassified, and unregulated, Clinics in Dermatology (2009) 27, 431–434.
[6] Vermeer BJ, Gilchrest BA. Cosmeceuticals. A proposal for rational definition, evaluation and regulation. Arch Dermatol (1996);132:337.
[7] Draelos ZD, The future of Cosmeceuticals: An Interview with Albert Kligman, MD, PhD
[8] Is It a Cosmetic, a Drug, or Both? (Or Is It Soap?), www.fda.gov
[9] 《什么是药妆品?》http://www.sfda.gov.cn/WS01/CL2014/179202.html
[10] 刘玮,《 药妆品的定义及法规定位—全球范围内的管理现状及问题思考》,中国医师协会.第4届中国美容与整形医师大会论文汇编,中国医师协会:,2007:1.